 中文
中文
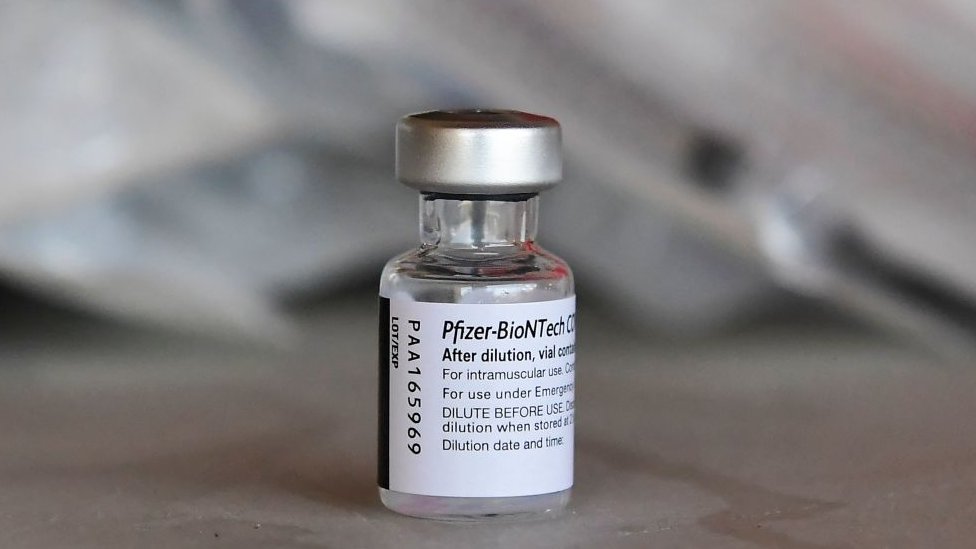
美國食品藥品監督管理局(FDA)已全面批准輝瑞/BioNTech新冠疫苗,這也是第一支在美國獲得全面授權的新冠疫苗。
美國此前授權該疫苗緊急使用,兩劑疫苗的接種間隔時間為三周。現在,這款疫苗已被完全批准用於16歲及以上人群。
對於12-15歲的群體,這款疫苗仍然只有緊急使用授權。
這一決定預計將使美國全國各地的僱主和組織更多地採取強制接種手段。這一決定的背景也是許多美國人對疫苗接種猶豫不決。
美國食品藥品監督管理局在一份聲明中說,其審查數據包括約4.4萬人的數據。輝瑞疫苗在預防新冠疾病方面有效率達到91%,該疫苗將以Comirnaty之名銷售。
美國食品藥品監督管理局代理局長珍妮特·伍德科克(Janet Woodcock) 說,「公眾可以非常有信心,這種疫苗在安全性、有效性和生產質量方面符合FDA要求的批准產品的高標凖。」

美國政府最初只給予輝瑞疫苗臨時授權,供16歲及以上的人使用。這意味著美國食品藥品監督管理局認為,在公共緊急衛生事件下使用這款產品的潛在好處大於風險。
輝瑞生物技術公司於5月初申請全面許可後不到4個月獲批,這是美國食品和藥物管理局100多年歷史上做出的最快的疫苗批准決定。
批評者一直呼籲美國食品藥品監督管理局加快這一審批程序,因為今年年初美國正努力解決疫苗接種率的問題。最近幾周,受新冠病毒變異毒株Delta重創的一些地區的疫苗接種率得到提升。
在周一(8月23日)的電視講話中,美國總統拜登直接喊話說:「你們一直等待的時刻到了……現在是你們去接種疫苗的時候了。今天就去接種吧。」
凱撒家庭基金會(Kaiser Family Foundation)在6月底發佈的民意調查數據顯示,大約30%未接種疫苗的美國人說,如果疫苗獲得FDA的全面批准,他們將更有可能接種疫苗。在對疫苗採取觀望態度的美國人中,這一數字上升到近50%。
美國食品藥品監督管理局宣佈全面授權後,美國軍方表示將正式要求所有130萬現役軍人接種該疫苗。
此外拜登呼籲私營公司和非營利機構要求員工接種疫苗。隨著美國開始恢復正常,美國的公司、醫療系統、大學和其他組織現在預計將要求接種疫苗。
迄今為止,有9200萬美國人完成了輝瑞疫苗接種,佔已完成新冠疫苗接種的美國人總數一半以上。
本網頁內容為BBC所提供, 內容只供參考, 用戶不得複製或轉發本網頁之內容或商標或作其它用途,並且不會獲得本網頁內容或商標的知識產權。

10/04/2024 10:44AM

09/04/2024 05:00PM

09/04/2024 05:00PM